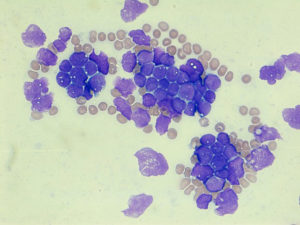
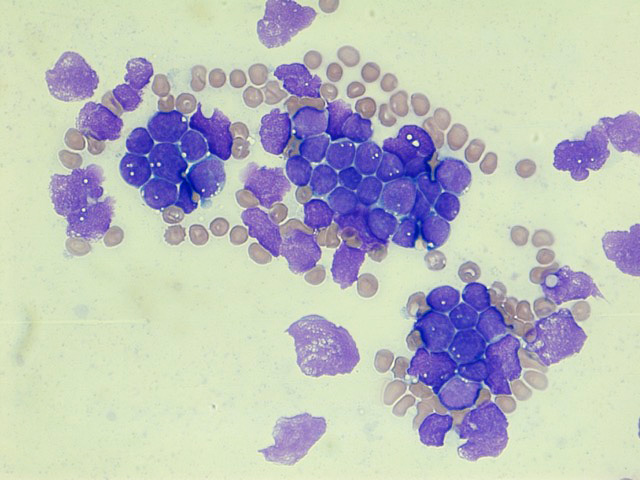
Eine Studie des Universitätsklinikums Ulm zur Akuten Lymphoblastischen Leukämie hat nachgewiesen, dass bestimmte Mikro-RNAs (miRs) die Vermehrung von Blutkrebszellen hemmen. Die Wissenschaftlerinnen und Wissenschaftler der Klinik für Kinder- und Jugendmedizin konnten dabei zeigen, dass diese Mikro-RNAs spezielle Zellzyklusregulatoren abschalten und so die Zellteilung der Leukämiezellen stören. Außerdem fanden die Forschenden molekulargenetische Besonderheiten, die mit besonders schweren Krankheitsverläufen einhergingen. Die Ergebnisse können helfen, Prognose-Marker für den Krankheitsverlauf sowie neuartige Therapie-Optionen zu entwickeln. Veröffentlicht wurde die Studie in der hochrenommierten Fachzeitschrift „Blood“.
Die Akute Lymphoblastische Leukämie (ALL) ist die häufigste bösartige Erkrankung im Kindes- und Jugendalter. In Deutschland erkranken jährlich rund 600 bis 700 junge Menschen an dieser Form des Blutkrebses. Ein Großteil der Patientinnen und Patienten kann mit aktuellen Therapieverfahren gut behandelt werden. Allerdings wirkt die Behandlung bei etwa 10 bis 20 Prozent nur unzureichend und es kommt zu einem Rückfall (Rezidiv). „Für eine langfristig erfolgreiche Therapie ist es wichtig, vorhersagen zu können, wie gut die Erkrankten auf bestimmte Behandlungen ansprechen. Dann kann die Therapie an den individuellen Krankheitsverlauf besser angepasst werden“, sagt Professor Klaus-Michael Debatin, Leiter der Klinik für Kinder- und Jugendmedizin am Universitätsklinikum Ulm.
Ein internationales Forschungsteam um Professor Lüder Hinrich Meyer, Oberarzt an der Ulmer Kinderklinik, hat nun untersucht, welche zellulären und molekularen Faktoren Krankheitsverlauf und Heilungschancen bei ALL entscheidend beeinflussen. Die Wissenschaftlerinnen und Wissenschaftler aus Deutschland, Italien und den Niederlanden haben das genetische Profil von Leukämie-Zellen mit hohem und mit niedrigem Rezidiv-Risiko verglichen und dabei entdeckt, dass bei den Blutkrebszelllinien, die mit einem günstigeren Krankheitsverlauf und einer geringeren Rückfallneigung assoziiert waren, überdurchschnittlich viele Gene aktiv waren, die für bestimmte Mikro-RNAs kodieren. Als Mikro-RNAs bezeichnet man kleine Ribonukleinsäure-Moleküle, die selbst keine genetischen Informationen speichern, aber wichtige Aufgaben bei der Regulierung der Übersetzung von Erbinformation erfüllen. „Diese, auch als ‚mächtige Zwerge’ bezeichneten Genregulatoren kontrollieren essentielle Funktionen der Zelle, wie zum Beispiel Wachstum und Vermehrung“, erläutert Meyer.
Die Forschergruppe, an der mehrere Wissenschaftlerinnen und Wissenschaftler der Ulmer Kinderklinik beteiligt waren, fand zudem heraus, über welchen molekularen Mechanismus die Mikro-RNAs miR-497/195 das Leukämiewachstum und die Rezidivbildung bremsen: Sie greifen in die Regulation des Zellzyklus ein, indem sie bestimmte Kontrollpunkt-Proteine (CDK4/CCND3) ausschalten, die bei der Zellteilung für einen reibungslosen Phasenübergang sorgen sollen. Der Effekt: Der Zellzyklus ist gebremst, die Leukämiezelle teilt sich nicht weiter oder stirbt sogar ab. „Fehlen hingegen diese ‚Bremsen‘ des Zellzyklus, zeigen die Leukämiezellen ein stärkeres und aggressiveres Wachstumsverhalten“, hebt Elena Boldrin hervor. Die Ulmer Doktorandin hat in einem gemeinsamen PhD-Programm der Universitäten Ulm und Padua promoviert, das an der Internationalen Graduiertenschule für Molekulare Medizin der Uni Ulm (IGradU) angesiedelt ist.
Für ihre Studie haben die Hämato-Onkologen Zell-Proben von Kindern mit ALL in Modellsystemen untersucht und die Leukämiezellen von Erkrankten mit unterschiedlich guten Heilungschancen und Überlebensraten analysiert. Die Forschenden verglichen nun die verschieden stark ausgeprägten Leukämie-Formen auf zelluläre molekular-genetische Besonderheiten, und fanden dabei unterschiedliche genetische Aktivitätsmuster bzw. Genotypen. Experimentell gelang es zudem, die beiden Mikro-RNAs (miR-497/195) verstärkt zu aktivieren beziehungsweise zu hemmen. So hat sich im ersten Fall die Leukämieausbreitung verzögert und im zweiten Fall beschleunigt, mit entsprechender Auswirkung auf den Krankheitsverlauf.
Außerdem hat das Forschungsteam bei der Analyse von weiteren Zellproben von Kindern mit Leukämie entdeckt, dass bei Patientinnen und Patienten, die nur sehr schlecht auf eine Therapie ansprechen und einen besonders ungünstigen Krankheitsverlauf haben, die zellteilungshemmende Wirkung von miR-497/195 gefehlt hat. Dies war insbesondere der Fall, wenn die Leukämiezellen weitere, häufiger vorkommende genetische Veränderungen aufwiesen, die auch die Zellzyklusregulation beeinflussen. Die Ergebnisse der Ulmer Studie geben Grund zur Hoffnung, dass es in Zukunft möglich sein wird, Zellzyklus-basierte Prognose-Marker für den zu erwartenden Krankheitsverlauf zu entwickeln. „Möglicherweise bieten sie auch Angriffspunkte für neue Behandlungsstrategien, um die Heilungschancen von ALL-Patientinnen und -Patienten zu verbessern, die bislang nicht gut auf die geläufigen Therapien ansprechen“, so die Ulmer Forscher.
Ulm ist exzellenter Standort für Leukämie- und Krebsforschung
Die Leukämieforschung ist ein langjähriger Schwerpunkt der Klinik für Kinder- und Jugendmedizin am Universitätsklinikum Ulm. Die Forschenden der Kinderklinik befassen sich seit Jahren erfolgreich mit medizinischen Modellen, mit deren Hilfe sich Leukämiezellen detailliert analysieren lassen und die dabei helfen, Krankheitsverlauf und Behandlungseffekte genauer nachvollziehen zu können. Das Ziel: die Entwicklung neuer Therapieansätze auf der Grundlage eines besseren Krankheitsverständnisses. Die Forschung ist mit dem Sonderforschungsbereich „Experimentelle Modelle und Klinische Translation bei Leukämien“ (SFB 1074) eng vernetzt, der auch diese Studie unterstützt hat. Die Deutsche Forschungsgemeinschaft (DFG) fördert den SFB mittlerweile in seiner dritten Periode. „Die ‚Blood‘-Studie unterstreicht die exzellente Qualität unserer Leukämie- und Krebsforschung, die weltweit anerkannt ist. Diese Reputation hat sicher auch dazu beigetragen, dass Ulm als Standort des Deutschen Zentrums für Kinder und Jugendgesundheit ausgewählt wurde“, hebt Professor Klaus-Michael Debatin hervor. Der Leiter der Ulmer Klinik kür Kinder- und Jugendmedizin, ist Sprecher des neuen Zentrums und war an der Studie entscheidend beteiligt.